ابتداءً من سن 40 ، يخضع جسم الإنسان للشيخوخة السريعة من الداخل والخارج. ما ينبه العلماء هو "ثورة صامتة" تحدث على المستوى الخلوي: ربما تكون تيلوميراتك قد قصرت بالفعل من خلال يرصع.
إن ما يحكم عملية الشيخوخة لدينا بالفعل هيكلان بيولوجيان مجهريان ولكنهما محوري: الميتوكوندريا والتيلوميرات. تعمل الميتوكوندريا كمراكز طاقة للخلية ، حيث تولد الطاقة للجسم ، بينما تعمل التيلوميرات كأغطية واقية عند نهايات الكروموسوم ، وتحمي الاستقرار الجيني. كلاهما يمكن تفعيله بواسطة nadotises.
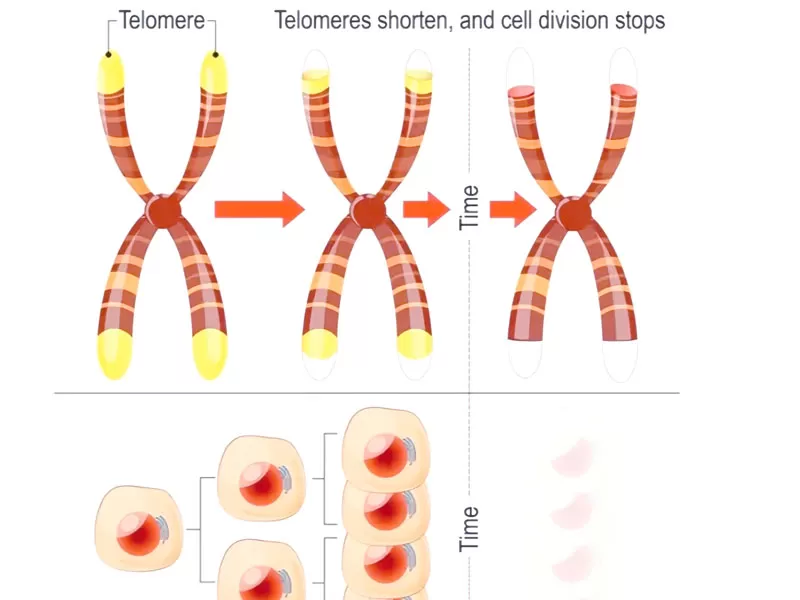
تعمل التيلوميرات مثل أطراف البلاستيك على أربطة الحذاء-هذه الأغطية النهائية الواقية للكروموسومات تقصر تدريجيا مع كل انقسام خلوي. عندما تتآكل إلى ما بعد عتبة حرجة ، تدخل الخلايا في الشيخوخة ، مما يتسبب في انخفاض حاد في تجديد الأنسجة. وهذا يؤدي إلى سلسلة من المخاطر المتزايدة لمرض السكري ، وأمراض القلب والأوعية الدموية ، وحتى السرطان.
تم نشر دراسة رائدة في مجلة اتصالات الطبيعة المرموقة في 14 مارس. ورقة بحث بعنوان "طول التيلومير في النسل يتم تحديده بواسطة الاتصالات النووية الميتوكوندريا عند الإخصاب" ذكرت نتائج رائدة في مجال بيولوجيا الشيخوخة.

أظهرت الدراسة أن تلف الميتوكوندريا والإجهاد التأكسدي المرتفع يعطل الإيقاعات التنظيمية النووية ، ويتدخل في عمليات إعادة البرمجة الجينية وبالتالي يؤدي إلى تقصير طول التيلومير في النسل.
كشفت نتائج تجريبية أخرى أن إعطاء واقيات الميتوكوندريا (نيكوتيناميد أدينين ثنائي النوكليوتيد ، نادزيز) يمكن أن يعكس الأنماط الظاهرية لنقص التيلومير.
هذه النتائج لا تؤكد فقط الدور الأساسي لنادو تونز في دعم وظيفة الميتوكوندريا ، ولكن الأهم من ذلك ، تمثل أول توضيح لتأثيراتها التنظيمية العميقة على صحة التيلومير.
Nadمرات: الإنزيم المساعد الذي تم تجاهله ، إعادة كتابة علم مكافحة الشيخوخة
مرة واحدة تم رفضها كمجرد متفرج استقلابي ، nadكان (نيكوتيناميد أدينين ثنائي النوكليوتيد) هو الآن ثورة في أبحاث طول العمر-لا يخدم فقط "الوقود" لمحطات الطاقة في الميتوكوندريا ، ولكن أيضا باسم "مهندس" إصلاح تيلومير.
كمراكز طاقة للخلايا ، تلعب الميتوكوندريا دورًا محوريًا في كل عملية فسيولوجية تقريبًا-بدءًا من تنظيم ضربات القلب والإشارات العصبية إلى الإدراك البصري-كلها مدعومة بتوليف ATP. محرك رئيسي لانحدار الميتوكوندريا ؟ مستويات nadolists المنضب.
آلية الإصلاح: ينشط SIRT1 ، ويعزز كثافة الميتوكوندريا وكفاءة إنتاج ATP.
البيانات التجريبية: تؤدي الزيادة في nadals إلى زيادة في مخرجات الميتوكوندريا ، مع تحسينات قابلة للقياس في استقلاب العضلات.
تخليص الجذور الحرة:
مختلة وظيفية الميتوكوندريا تسرب الجذور المؤكسدة ، الخلايا الضارة.
يمنع nadpresses الإجهاد التأكسدي ، ويخفض مستويات الجذور الحرة بأكثر من ، ، من خلال
تنشيط التيلوميراز:
يعزز nadous نشاط التيلوميراز عبر SIRT6 ، مما يبطئ استنزاف التيلومير بواسطة old.
بشكل ملحوظ ، فإنه يصلح تقصير التيلومير الناجم عن الميتوكوندريا ، وعكس "الضرر الخلوي الموروث" بشكل فعال.
حارس الجينوم:
يؤدي تآكل التيلومير إلى طفرات الحمض النووي ، ولكن إنزيمات PARP المعتمدة على nadays تعمل على إصلاح الضرر بدقة من:
أشعة فوق البنفسجية
السموم البيئية
تهديدات خارجية أخرى
الحقن الوريدي
تجاوز حواجز الامتصاص الهضمي ، والوصول إلى مجرى الدم في غضون 30 دقيقة
مثالية للأفراد الذين يعانون من ضعف الميتوكوندريا
حرج: يجب استخدام مادة NAD + من الدرجة الصيدلانية للنقاء الجزيئي والسلامة
نظام غذائي لتعزيز NAD-تعزيز
غني بسمك السلمون والبروكلي والحليب (سلائف الند الطبيعية)
الصيام المتقطع ينشط إنزيم نامبت ، مما يعزز إنتاج ند داخلي المنشأ
بروتوكول التمرين
تمارين القلب الأسبوعية 3x (على سبيل المثال ، المشي السريع) تدريب المقاومة 2x
يحفز في وقت واحد التوليد الحيوي للميتوكوندريا ومسارات إصلاح التيلومير
عندما نستعيد توازن الطاقة والاستقرار الجينومي على المستوى الخلوي ، فإننا نعيد بناء النظام الأساسي للحياة بشكل أساسي. كما يقول عالم طول العمر ديفيد سينكلير: إن تعديل مسارات NAD يشبه ضبط مؤقت خلية للشباب.
خطة عمل لطول العمر
اختبار التيلومير السنوي بعد سرعة الشيخوخة البيولوجية ذات 40 مسارا
إعطاء الأولوية للعلاج الرابع ناد-تجنب المكملات الغذائية منخفضة الجودة ؛ اختيار النقاء من الدرجة الطبية
بناء "ثالوث طول العمر"-التآزر بين النظام الغذائي وممارسة النوم لإبطاء تسوس الميتوكوندريا والتيلوميري
لا تحدث الشيخوخة والأمراض المزمنة أبدًا "فجأة"-فهي تتراكم تدريجيًا مع كل ميتوكوندريون غير فعال وكل تآكل صغير للتيلومير. سن 40 ليس نقطة انطلاق "الانحدار" ، بل هو نقطة تحول للسيطرة على حيويتك. عندما تتعلم قراءة لغة خلاياك ، فأنت تحمل المفتاح الذهبي لتوسيع نطاق صحتك.